组织透明3D成像可视化胚胎&胎盘发育
在生命科学领域,对器官三维结构的精准解析一直是探索生理与病理机制的核心目标。传统组织学方法依赖二维切片重建,难以完整保留器官结构且易受操作变形影响。而新兴的组织透明化技术结合光片显微镜,为解决这一难题提供了全新路径。2017年发表于《Scientific Reports》的一项研究,通过改良的CUBIC组织透明化方法,成功实现了小鼠子宫内胚胎与胎盘的三维可视化,为深入理解胎盘发育及相关疾病机制奠定了基础。

研究背景与技术挑战
在该研究之前,科研人员主要依靠传统的组织切片和染色技术来分析子宫和胎盘的结构。这些方法需要制备大量连续的薄组织切片,然后通过染色来观察细胞和组织结构。然而,这种方法存在明显的局限性。首先,在切片过程中,组织很容易发生变形。其次,染色过程也可能破坏组织的完整性。染色剂可能无法均匀地渗透到组织的各个部分,导致某些区域的染色效果不佳,影响对细节的观察。此外,通过二维切片来重建三维结构是一项非常复杂且耗时的工作。因此,传统方法在分析子宫和胎盘的三维结构时面临着巨大的挑战。
子宫和胎盘的结构具有很强的特殊性,这使得传统的成像方法难以有效应用。子宫是一个肌肉丰富的器官,其肌肉组织的存在会对光线的穿透造成阻碍。而胎盘则是一个血管密集的器官,富含血液和血管,这使得光线在穿透胎盘时会被大量吸收和散射,导致成像效果不佳。具体来说,子宫的肌肉组织中含有大量的肌红蛋白,而胎盘的血管中含有大量的血红蛋白。这些色素分子会吸收特定波长的光线,使得传统的光学成像技术难以穿透这些组织,从而无法获取清晰的内部结构图像。
技术创新与应用
在这项研究中,科研人员选择了CUBIC方法,并对其进行了改良,以适应子宫和胎盘的特殊结构。CUBIC方法的核心在于其独特的试剂配方,能够有效地去除组织中的色素分子,如血红蛋白和肌红蛋白,同时保持组织的完整性和荧光标记的稳定性。
CUBIC试剂由多种成分组成,这些成分相互作用,能够溶解和去除组织中的脂类和色素,同时保持组织的三维结构。与其他组织透明化方法相比,CUBIC方法具有明显的优势。首先,它能够高效地去除子宫和胎盘中的血红蛋白和肌红蛋白,使组织变得透明,从而允许光线穿透,进行三维成像。其次,CUBIC方法对组织的损伤较小,能够较好地保持组织的结构和抗原性,为后续的免疫组织化学染色等分析提供了可能。此外,CUBIC方法的处理时间相对较短,能够在较短的时间内完成组织透明化处理,提高了实验效率。
光片显微镜是一种新型的光学成像技术,与传统的共聚焦显微镜相比,具有更高的成像速度和更深的穿透能力。在这项研究中,科研人员将改良的CUBIC方法与光片显微镜相结合,实现了对子宫和胎盘的三维成像。光片显微镜的工作原理是利用一束薄的激光片来照射样本,从而激发样本中的荧光标记分子,然后通过相机收集发射的荧光信号,形成二维图像。通过对样本进行逐层扫描,可以获取一系列的二维图像,然后通过计算机处理,重建出样本的三维结构。
光片显微镜的优势在于其能够在较短的时间内获取高分辨率的三维图像,同时对样本的损伤较小。这使得它非常适合用于对活体样本或脆弱的组织样本进行成像。在这项研究中,光片显微镜被用于对透明化的子宫和胎盘进行成像,成功获取了胚胎和胎盘的三维结构图像,为后续的分析提供了高质量的数据。
为了进一步提高成像的对比度和特异性,科研人员还结合了多种标记技术。例如,他们使用了荧光核染色剂碘化丙啶(PI)来标记细胞核,从而能够清晰地观察到细胞的分布和排列。此外,他们还利用转基因小鼠,将增强型绿色荧光蛋白(EGFP)标记在胚胎和胎盘的特定细胞上,从而能够特异性地追踪这些细胞的位置和迁移路径。通过这些多模态标记技术的结合,科研人员能够更加清晰地观察到子宫和胎盘中的各种结构和细胞,为深入分析胚胎和胎盘的发育过程提供了有力的工具。
成像实验与结果分析
样本制备:实验选用了不同孕期的小鼠子宫和胎盘作为研究对象。首先,对小鼠进行深度麻醉,然后通过心脏灌注4%多聚甲醛(PFA)/磷酸盐缓冲液(PBS)和碘化丙啶(PI)溶液,对组织进行固定和染色。固定完成后,将子宫和胎盘组织分离出来,进一步在4%PFA中浸泡过夜,以确保组织充分固定。
CUBIC透明化处理:将固定好的组织浸泡在CUBIC-1试剂中,在37°C下温和振荡处理3天。之后更换新鲜的CUBIC-1试剂,继续处理2天。这一步骤的目的是去除组织中的脂类和色素,使组织变得透明。处理完成后,用PBS对组织进行3次清洗,每次清洗在室温下温和振荡进行。接着,将组织浸泡在20%蔗糖的PBS溶液中1天,进行脱水处理。最后,将组织浸泡在CUBIC-2试剂中2天,进一步优化组织的透明度和折射率。
光片显微镜成像:将透明化处理后的组织样本置于光片显微镜下进行成像。使用物镜获取整个生殖器官的整体图像、具有单细胞分辨率的详细图像。在成像过程中,使用638nm的激发波长来激发组织中的自发荧光信号,同时结合PI和EGFP的荧光标记,获取高质量的三维图像。
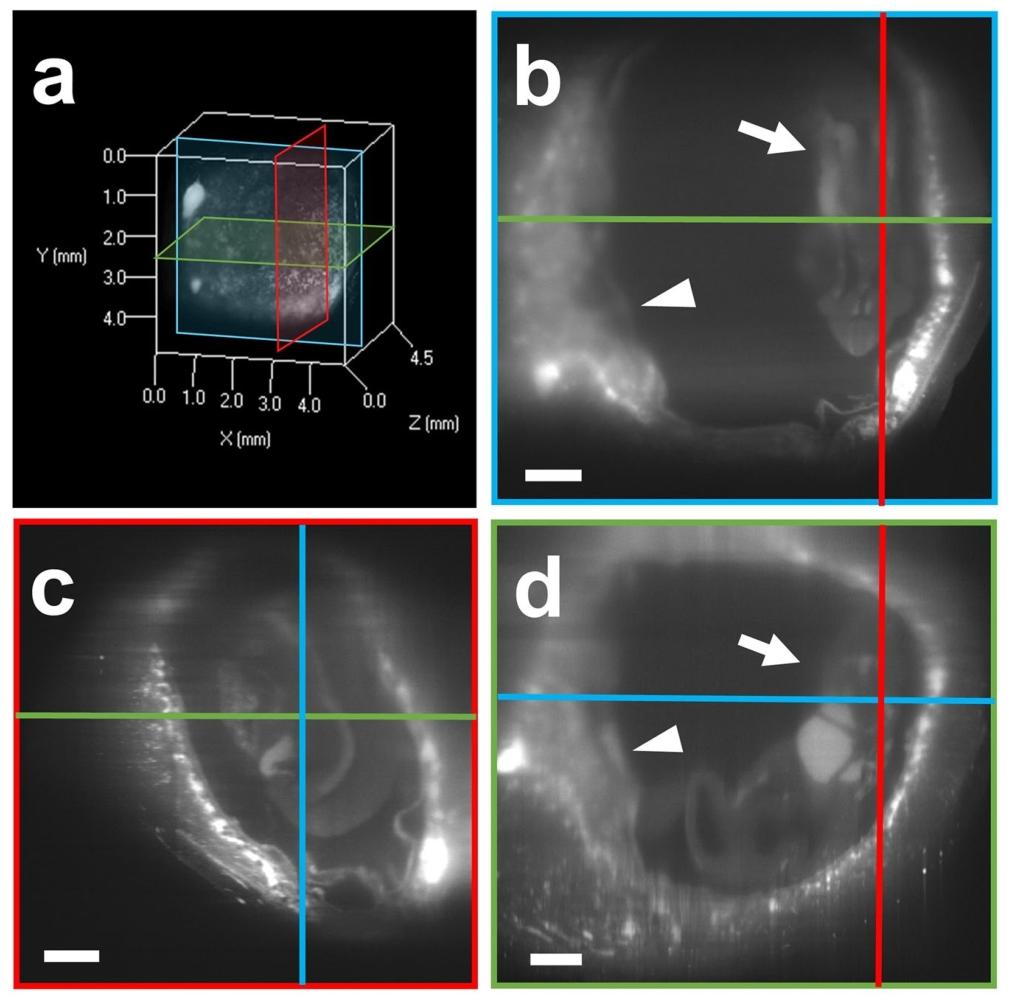
用光片显微镜观察怀孕子宫的宫内结构
图像分析与处理:使用ZEN软件对获取的三维图像进行分析和处理。通过三维重建和图像处理技术,科研人员能够从不同角度观察子宫和胎盘的结构,获取各种截面图像,并进行定量分析。
透明化子宫与胎盘的三维结构:通过CUBIC透明化处理和光片显微镜成像,科研人员成功获取了小鼠子宫和胎盘的三维透明图像。在E9.5的子宫图像中,可以清晰地看到胚胎和胎盘的大致轮廓,以及它们在子宫内的位置关系。随着孕期的推进,在E14.5的胎盘图像中,可以观察到更加复杂的血管结构和细胞分布。这些图像不仅展示了子宫和胎盘的整体形态,还揭示了其内部的精细结构,为进一步研究提供了直观的数据。
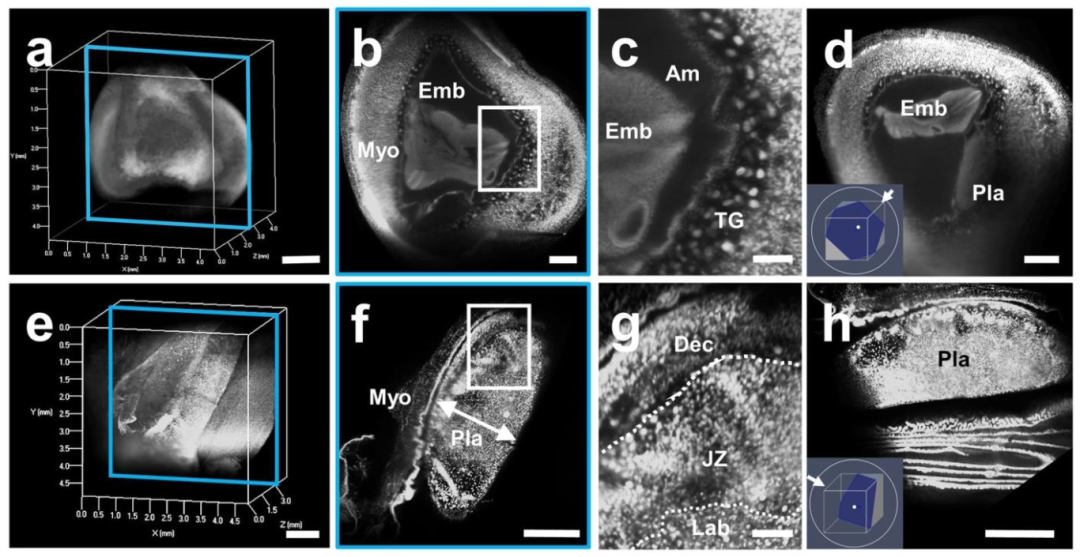
用PI染色的怀孕子宫和胎盘的三维和横截面图像
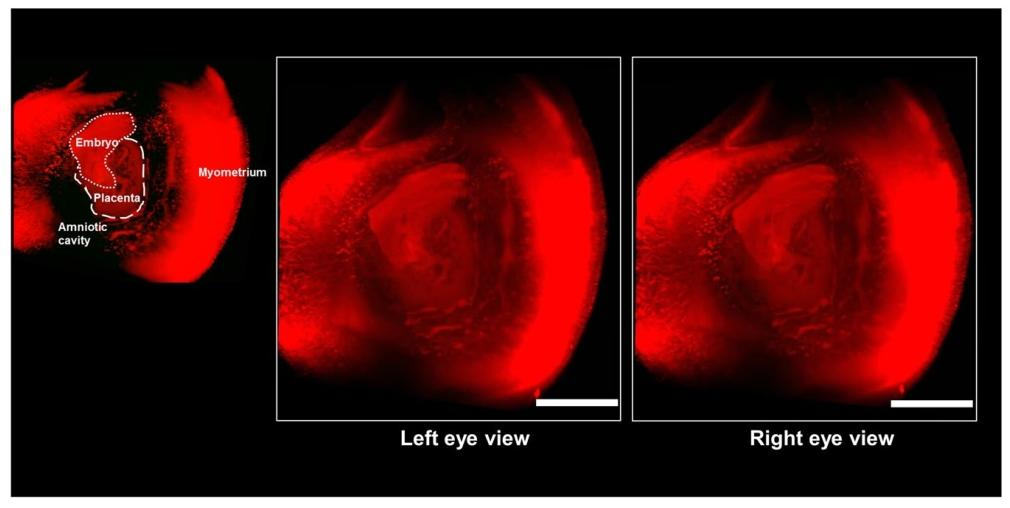
用PI染色的怀孕子宫立体图像
细胞核与特定细胞的定位:利用PI染色,科研人员成功标记了子宫和胎盘中的细胞核。通过三维成像,可以清晰地看到细胞核在组织中的分布情况,以及细胞的排列方式。此外,结合EGFP转基因小鼠,科研人员能够特异性地标记胚胎和胎盘的特定细胞,如滋养层细胞。通过观察EGFP标记的细胞,科研人员能够追踪这些细胞在子宫内的迁移路径,以及它们与母体组织的相互作用。
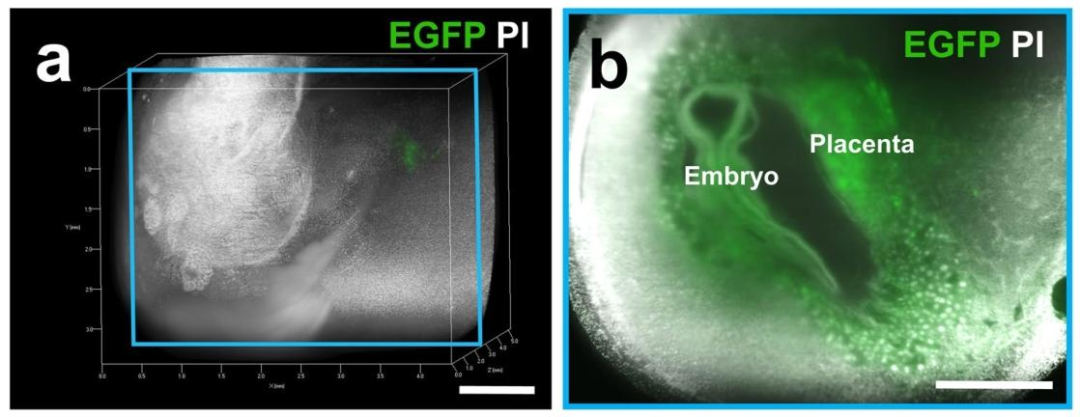
野生型小鼠子宫中EGFP阳性概念的三维图像
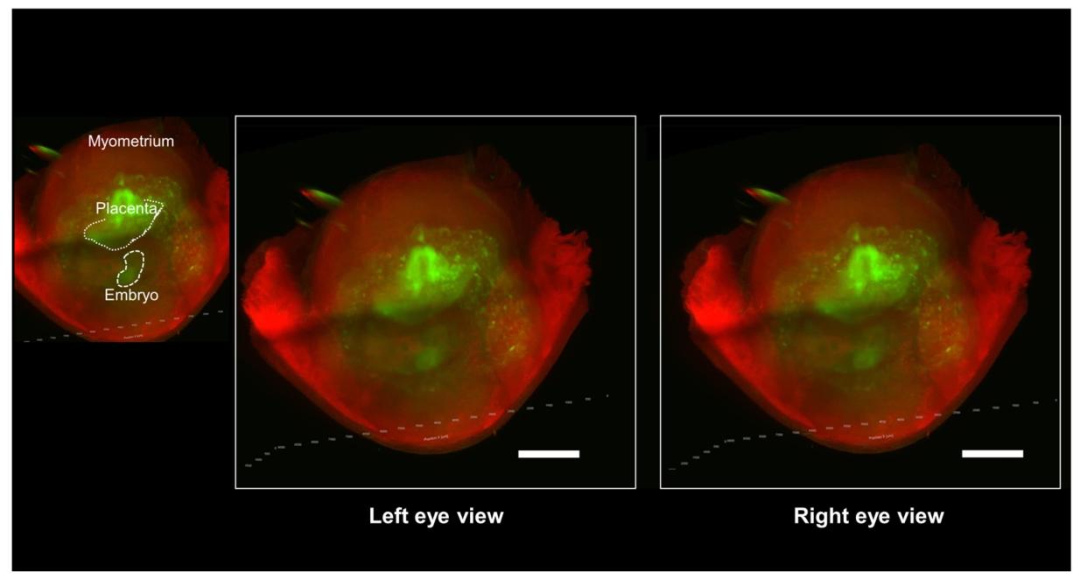
野生型小鼠EGFP阴性子宫中EGFP阳性概念的立体图像
免疫组织化学验证:为了验证成像结果的准确性,科研人员对透明化的组织样本进行了免疫组织化学染色。他们选择了血管内皮标记物CD31和滋养层标记物细胞角蛋白-7(CK7)进行染色。在染色后的组织切片中,能够清晰地观察到CD31和CK7的阳性信号,这表明CUBIC透明化处理并没有破坏组织的抗原性,为后续的免疫组织化学分析提供了可能。
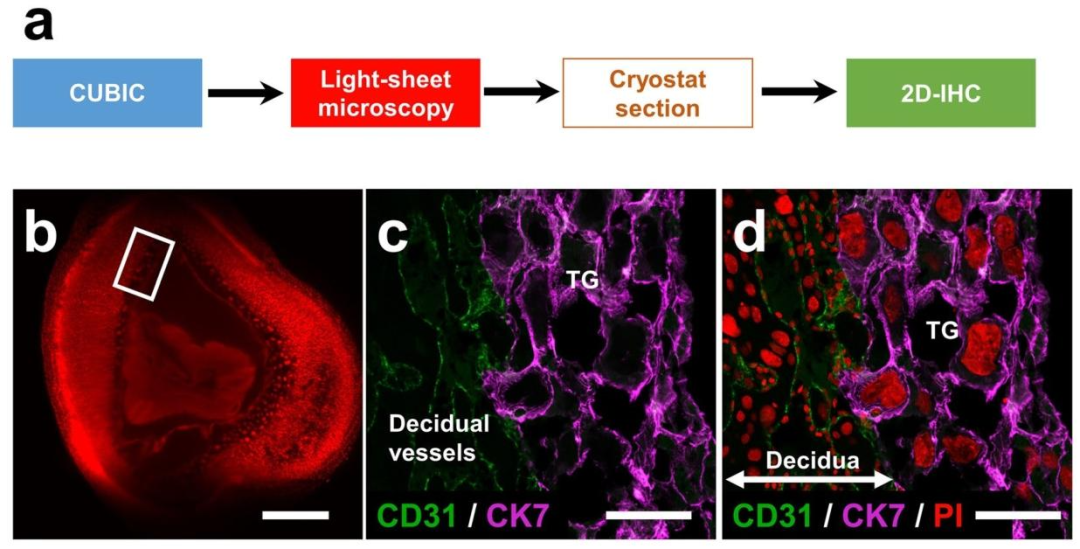
来自透明妊娠子宫器官阻滞的组织切片的免疫组织化学染色
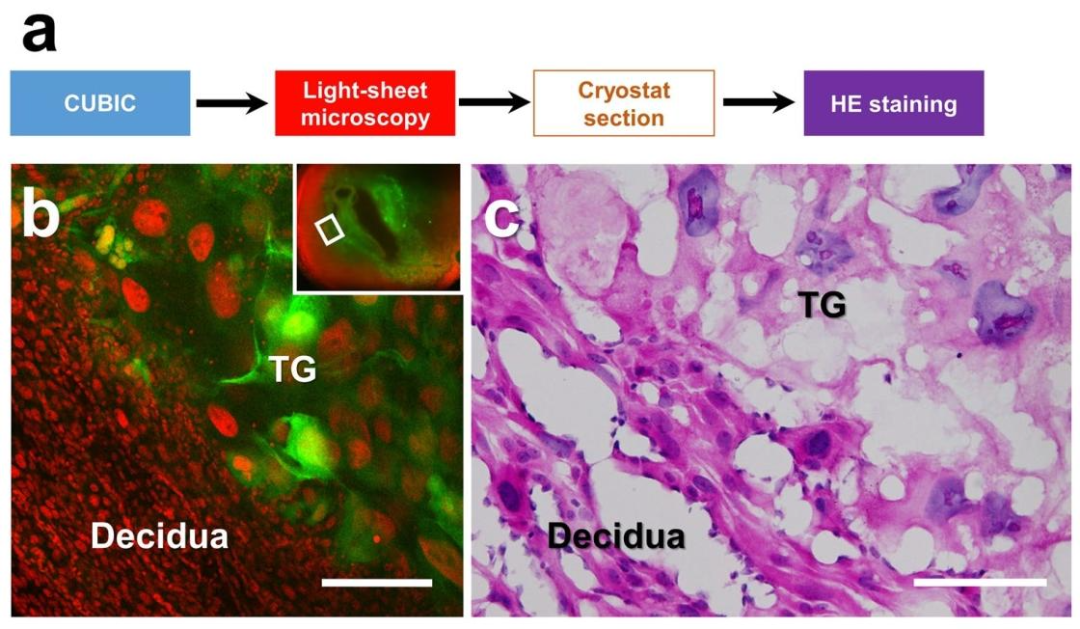
通过准备相应的组织切片对透明器官块进行组织学分析
总结与展望
通过改良CUBIC组织透明化技术与光片显微镜结合,首次实现了小鼠子宫内胚胎与胎盘的三维可视化,突破了传统组织学方法的局限。研究发现,优化后的CUBIC方案能有效消除子宫肌红蛋白和胎盘血红蛋白的干扰,保留组织完整性,并通过PI染色和EGFP转基因技术实现细胞核与特定细胞的精准定位。光片显微镜的应用进一步提供了单细胞分辨率的三维成像能力,揭示了胚胎与胎盘在子宫内的空间分布及动态发育过程,为胎盘血管重塑、滋养层细胞侵袭等关键机制研究奠定了基础。
然而,PI在胚胎深部的染色效率不足,晚期胎盘组织的成像分辨率有待提升,且人类样本的适用性尚未验证。未来研究可聚焦于技术优化,开发更高效的染色策略(如原位杂交或新型荧光探针),提升深层组织标记效果,探索CUBIC与超分辨显微镜的结合,突破光学衍射极限。
声明:本文仅用作学术目的。
Kagami, K., Shinmyo, Y., Ono, M. et al. Three-dimensional visualization of intrauterine conceptus through the uterine wall by tissue clearing method. Sci Rep 7, 5964 (2017).
DOI:10.1038/s41598-017-06549-6.
关注光量科技
Copyright LogiScience Technology Co.,Ltd 2021. All Rights Reserved.
武汉光量科技有限公司


